■ 미토콘드리아 DNA, 새 유전자 가위 개발
● IBS 연구단, 새로운 핵과 미토콘드리아 DNA 염기 교정 기술 개발
미토콘드리아(mitochondria) DNA를 더 다양하고 더 정확하게 교정할 수 있는 길이 열렸다. 기초과학연구원(IBS) 유전체 교정 연구단은 새로운 핵과 미토콘드리아 DNA 염기 교정 기술인 징크 핑거 염기 교정 효소(ZFD. Zinc Finger Deaminase) 개발에 성공했다. 미토콘드리아(mitochondria)는 에너지를 만들어내는 세포 내 소기관이다. 미토콘드리아(mitochondria) DNA에 변이가 일어나면, 시력. 청력뿐 아니라 중추 신경계. 근육. 심장 등에 치명적 결함을 불러온다.
미토콘드리아(mitochondria) 질환은 5천명 중 한 명 꼴로 발생하는 비교적 흔한 유전 질환이다. 현재 유전체 교정 기술로 널리 활용되는 크리스퍼 유전자 가위(CRISPR-Cas9)로는 미토콘드리아 DNA 교정이 불가능하다. 2020년 세균 유래 DddA 탈아미노 효소와 탈이펙터 단백질을 이용한 새로운 염기 교정 효소 DdCBE가 개발됐는데, 이는 유일한 미토콘드리아 DNA 염기 교정 기술이었다.
연구팀은 기존의 DddA 탈아미노 효소와 징크 핑거 단백질(Zinc finger protein)을 융합해 새로운 핵과 미토콘드리아 DNA 염기교정 기술인 징크 핑거 염기 교정 효소(Zinc Finger Deaminase)를 개발했다. 징크 핑거 단백질(Zinc finger protein)은 기존에 사용된 탈이펙터 단백질보다 크기가 절반 이상 작아 다양한 구조로 디자인할 수 있고 활용이 쉽다. 세포 투과 능력이 있어서 핵산 없이도(nucleic acid-free) 유전체 교정이 가능한 장점도 있다.
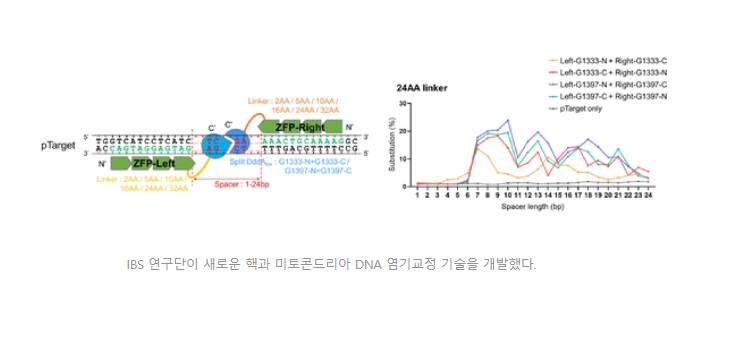
연구팀은 우선 24개의 징크 핑거 염기 교정 효소(Zinc Finger Deaminase) 구조 쌍을 제작해 최적의 구조를 찾아냈다. 이어 징크 핑거 염기 교정 효소(Zinc Finger Deaminase)를 이용해 핵과 미토콘드리아 DNA의 시토신/구아닌(C/G) 염기쌍을 티민/아데닌(T/A)으로 치환하는 데 성공했다. 개발한 징크 핑거 염기 교정 효소(ZFD. Zinc Finger Deaminase)나 ZFD-DdCBE 하이브리드(ZFD-DdCBE hybrid)를 사용하면, 기존의 DdCBE만으로는 만들 수 없었던 변이를 다양하게 유도할 수 있다.
김진수 단장은 “앞으로 미토콘드리아 질환을 비롯한 난치병 연구와 치료뿐 아니라 식물의 엽록체 DNA 등 다른 소기관의 DNA 교정에도 다양하게 활용될 것이다. 징크 핑거 염기 교정 효소(Zinc Finger Deaminase)는 작은 크기 덕분에 세포 전달에 많은 이점이 있는 만큼 여러 기술들과 접목해 활용도가 클 것으로 기대된다”고 말했다. 연구 결과는 생물학 분야의 국제학술지 Nature communications 2022년 01월 18일자 온라인 판에 실렸다.
■ 남이 보지 못하는 것을 보는 것이 비젼(Vision)이다. ★ 건강 관련 자료 및 혁신적인 문화 소식을 소개하고 공유하고자 합니다. ★ 그래서, → ★ 젊음(靑春), 생명공학의 열망(熱望)! 네이버 밴드로 초대합니다.
→ http://www.band.us/#!/band/55963286
'건강 (Bio 혁명)' 카테고리의 다른 글
| ■ 특정 인지질이 세포의 생사를 결정 짓는다. (0) | 2022.02.27 |
|---|---|
| ■ 모든 혈액형에 이식 가능한 O형 장기 제작 성공 (0) | 2022.02.22 |
| ■ 미토콘드리아에 약물 전달 수송체 새로 개발 (0) | 2022.01.23 |
| ■ 암 패혈증 등에서 혈관 정상화하는 항체 개발 (0) | 2021.11.01 |
| ■ 스마트폰 카메라에 손가락만 대면 혈압 측정 (0) | 2021.10.13 |
